Tổng quan, vai trò, sự nhiễm trùng và phản ứng HBV
Bài viết sau đây chúng ta cùng tìm hiểu về Tổng quan, vai trò, sự nhiễm trùng và phản ứng HBV. Sự tái hoạt của virus viêm gan B (HBVr) có thể xảy ra ở những bệnh nhân được điều trị bằng liệu pháp ức chế miễn dịch và hóa trị. Do đó, trong thời đại sinh học hiện nay, các bác sĩ cần hiểu rõ nguy cơ tái hoạt của virus viêm gan B ở những bệnh nhân mắc bệnh tự miễn đang điều trị bằng liệu pháp kháng cytokine.
1. Tổng quan
Ba thành phần sau đây rất quan trọng đối với phát triển của sự tái hoạt virus viêm gan B:
Đáp ứng miễn dịch của vật chủ;DNA tròn khép kín cộng hóa trị của bộ gen virus HBV (cccDNA);Việc sử dụng thuốc ức chế miễn dịch.
Nhiễm HBV gây ra một loạt các bẩm sinh và thích nghi phản ứng miễn dịch. Các phản ứng miễn dịch của vật chủ chống lại sự lây nhiễm của virus viêm gan B (HBV) cho phép các tế bào T (Tc) gây độc tế bào thích ứng để tạo ra cả tác dụng kháng virus, phụ thuộc vào phân bào và không phụ thuộc vào chỉ định.
Trong tác dụng không phụ thuộc vào phân bào, interferon (IFN) đóng một vai trò quan trọng để ngăn chặn sự nhân lên của HBV. Để tạo ra các kháng thể trung hòa với HBV trong tuần hoàn, các tế bào B cũng được tuyển chọn để hạn chế sự lây lan của virus HBV. Tuy nhiên, ngay cả khi đạt được kết quả phân tích lâm sàng về nhiễm HBV, điều đó không có nghĩa là loại bỏ hoàn toàn HBV-DNA vì cccDNA có thể tồn tại trong nhân tế bào gan và nó có thể là nguồn cung cấp sự tái hoạt của virus viêm gan B khi sử dụng thuốc ức chế miễn dịch.
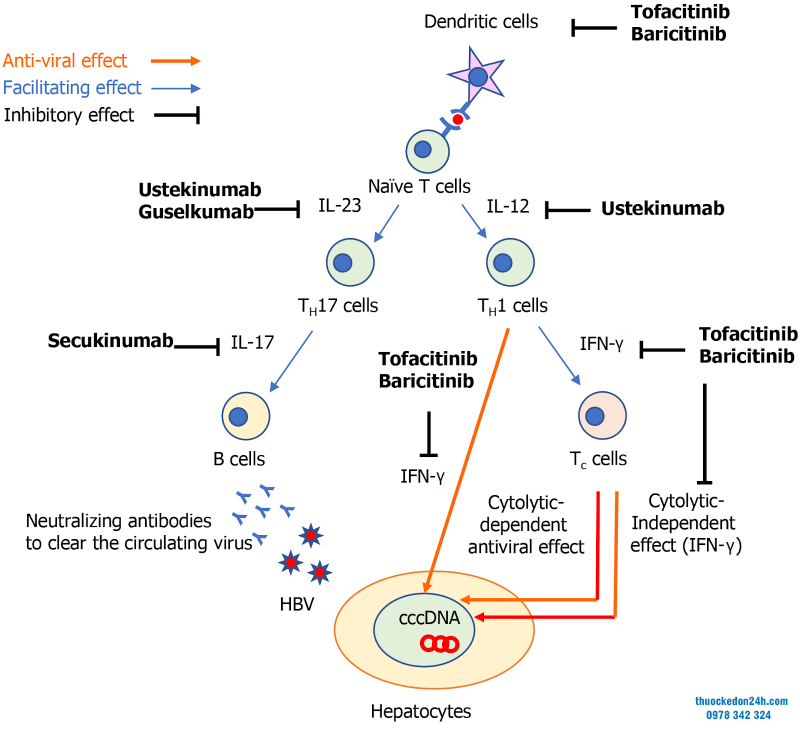
Cơ chế miễn dịch có thể có để giải thích cách sinh học nhắm mục tiêu vào yếu tố hoại tử không phải khối u có thể gây ra sự tái hoạt của virus viêm gan B.
2. Vai trò của yếu tố hoại tử khối u (TNF) -α
Yếu tố hoại tử khối u (TNF) -α là cytokine quan trọng không chỉ trong cơ chế bệnh sinh của các bệnh tự miễn mà còn trong các phản ứng miễn dịch của vật chủ chống lại nhiễm HBV. TNF-α được tổng hợp bởi đại thực bào, tế bào T và tạo ra nhiều loại cytokine gây viêm, ngăn chặn sự nhân lên của virus. TNF-α cũng cần thiết cho sự tăng sinh của các tế bào Tc đặc hiệu với HBV cần thiết để ức chế sự nhân lên của HBV. Do đó, các chất ức chế TNF-α (ví dụ như infliximab, adalimumab và etanercept) có thể ức chế phản ứng miễn dịch kháng HBV, dẫn đến sự nhân lên của HBV. Tỷ lệ lưu hành chung của sự tái hoạt của virus viêm gan B ở những bệnh nhân mắc các bệnh tự miễn đang điều trị thuốc ức chế TNF-α được báo cáo là 4,2% (KTC 95%: 1,4% -8,2%).
Các con đường tín hiệu liên quan đến interleukin (IL) -12/23, IL-17 và Janus kinases (JAKs) đã được đánh dấu là mục tiêu điều trị cụ thể mới cho các bệnh tự miễn. Một nghiên cứu quan sát đa trung tâm gần đây đối với bệnh vảy nến cho thấy, sự tái hoạt của virus viêm gan B phổ biến hơn ở những bệnh nhân được điều trị bằng thuốc kháng TNF-α so với thuốc ức chế IL-17. Tuy nhiên, vẫn còn ít dữ liệu trong việc hiểu về nguy cơ tái hoạt của virus ở những bệnh nhân được điều trị bằng sinh học ức chế các con đường viêm cụ thể như vậy.
3. Sự nhiễm trùng và phản ứng của viêm gan B
Các hiệp hội nghề nghiệp ở Hoa Kỳ [Hiệp hội Nghiên cứu Bệnh gan Hoa Kỳ (AASLD); Hiệp hội Tiêu hóa Hoa Kỳ (AGA)], Châu Âu [Hiệp hội Nghiên cứu Gan Châu Âu (EASL)] và Châu Á [Hiệp hội Nghiên cứu Gan Châu Á Thái Bình Dương (APASL)] đã xuất bản các hướng dẫn để hỗ trợ các nhà cung cấp quản lý sự tái hoạt của virus viêm gan B. Cụ thể:
HBV mãn tính: HBV mãn tính (CHB) [ tức là, kháng nguyên bề mặt viêm gan B (HBsAg) – dương tính và kháng thể với kháng nguyên lõi viêm gan B (anti-HBc) – dương tính] bao gồm những bệnh nhân có hoạt động mãn tính [HBV DNA huyết thanh ≥ 2000 IU/ mL và bình thường hoặc tăng alanin transaminase (ALT) trong huyết thanh] hoặc không hoạt động (HBV DNA huyết thanh <2000 IU /mL và nhiễm HBV ALT bình thường).HBV đã hồi phục: HBV đã hồi phục (tức là chỉ số HBsAg âm tính và anti-HBc dương tính). Lưu ý, không có đủ bằng chứng để hỗ trợ việc sử dụng hiệu giá kháng HBs như một biện pháp hỗ trợ quyết định khi đưa ra khuyến nghị về điều trị dự phòng.
Có sự khác biệt nhỏ về định nghĩa sự tái hoạt của virus giữa các hướng dẫn, tuy nhiên khái niệm chung là giống nhau. Ở bệnh nhân HBV mãn tính, sự tái hoạt của virus viêm gan B được xác định bằng sự gia tăng HBV DNA trên mức cơ bản. Ở những bệnh nhân có HBV đã phân giải, sự tái hoạt của virus được xác định bằng sự xuất hiện của HBV DNA trong máu hoặc chuyển đổi sang trạng thái HBsAg + (tức là chuyển đảo huyết thanh).
Sự không đồng nhất quan sát được trong định nghĩa tái hoạt của virus cũng được phản ánh trong các nghiên cứu hiện có về sự tái hoạt của virus viêm gan B. Phần lớn các nghiên cứu bao gồm các thông số sau:
Mức độ HBV-DNA tăng nhanh so với ban đầu;Tăng nồng độ aminotransferase huyết thanh;Đảo ngược huyết thanh.
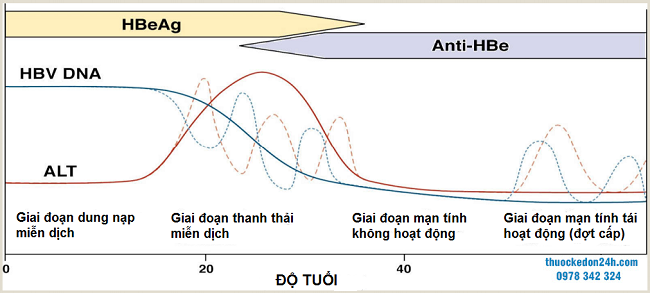
HBV mãn tính và các giai đoạn khác nhau
4. Quản lý bệnh nhân nhiễm virus viêm gan B đang điều trị miễn dịch
4.1. Phân cấp rủi ro
Bệnh nhân HBV mãn tính tăng nguy cơ mắc sự tái hoạt của virus viêm gan B khi điều trị bằng liệu pháp ức chế miễn dịch so với những bệnh nhân có HBV đã phân giải. Ví dụ, trong số những bệnh nhân được điều trị bằng thuốc ức chế TNF-α, ước tính có nguy cơ sự tái hoạt của virus viêm gan B tăng gấp 5 lần ở những bệnh nhân HBV mãn tính so với bệnh nhân HBV đã hồi phục (15,4% so với 3,0% nguy cơ sự tái hoạt của virus viêm gan B).
Một nghiên cứu khác cho thấy tỷ lệ tổng hợp sự tái hoạt của virus viêm gan B mà không được điều trị dự phòng bằng thuốc kháng virus là 15,6% (KTC 95%: 2,3-35,7) ở bệnh nhân HBV mãn tính được điều trị bằng thuốc ức chế TNF-α. Ở những bệnh nhân có HBV đã giải quyết, tỷ lệ gộp chung sự tái hoạt của virus viêm gan B mà không được điều trị dự phòng bằng thuốc kháng vi-rút ở những bệnh nhân được điều trị bằng thuốc ức chế TNF-α cũng như điều trị sinh học không nhắm mục tiêu TNF là 1,4% (KTC 95%: 0,5% -2,6%) và 6,1% (95 % CI: 0,0% -16,6%), tương ứng.Tiếp theo, cần đánh giá mức độ ức chế miễn dịch do chất sắt dự kiến. Những người nhận ghép tế bào gốc tạo máu (HSCT) và các liệu pháp làm suy giảm tế bào B (ví dụ như rituximab) là những phác đồ có hiệu lực cao và nguy cơ mắc tái hoạt của virus viêm gan B cao nhất. Các hướng dẫn của AGA khẳng định rằng, anthracycline (ví dụ như doxorubicin) và corticosteroid liều trung bình đến cao (CS) (tức là ≥ 10 mg prednisone hàng ngày hoặc tương đương trong ≥ 4 tuần) gây ra nguy cơ cao hơn so với các thuốc ức chế miễn dịch khác.
4.2. Điều trị dự phòng
HBV mãn tính
Nói chung, các hướng dẫn xã hội nghề nghiệp khuyến nghị điều trị dự phòng HBV, điển hình là entecavir hoặc tenofovir, cho tất cả các ứng viên ức chế miễn dịch có HBV mãn tính, ngoại trừ những bệnh nhân được điều trị bằng các thuốc ức chế miễn dịch truyền thống (ví dụ: thiopurine, methotrexate), CS nội khớp hoặc đường uống CS ≤ 1 tuần. AGA phân tầng nhóm bệnh nhân này thành nhóm nguy cơ vừa (1% -10%) và nhóm nguy cơ cao (> 10%) đối với sự tái hoạt của virus viêm gan B. Điều trị dự phòng kháng virus nên được bắt đầu trước và tiếp tục sau khi ngừng ức chế miễn dịch, thường là 12 đến 18 tháng nếu sử dụng các liệu pháp hiệu lực cao và 6 đến 12 tháng đối với các liệu pháp khác.
HBV đã hồi phục
Các hướng dẫn phần lớn đồng ý rằng bệnh nhân HBV đã hồi phục bằng phương pháp ức chế miễn dịch hiệu lực cao (người nhận HSCT và liệu pháp làm suy giảm tế bào B) nên được điều trị dự phòng sự tái hoạt của virus viêm gan B. AGA xếp nhóm bệnh nhân này vào nhóm sự tái hoạt của virus viêm gan nguy cơ cao (> 10%).Đối với bệnh nhân HBV đã hồi phục không theo phác đồ hiệu lực cao, các hướng dẫn khác nhau hơn. AGA khuyến nghị điều trị dự phòng cho những bệnh nhân HBV đã hồi phục có nguy cơ vừa (1% -10%) sự tái hoạt của virus viêm gan B, bao gồm những bệnh nhân được điều trị bằng chất ức chế TNF-α, chất ức chế cytokine khác hoặc chất ức chế tích phân, tyrosine kinase, CS liều trung bình hoặc cao cho ≥ 4 wk cũng như các dẫn xuất anthracycline.
Ngược lại, AASLD, EASL và APASL khuyến nghị một liệu pháp ưu tiên cho nhóm bệnh nhân này, không phải điều trị dự phòng. Theo đó, theo dõi phòng thí nghiệm nối tiếp (HBV DNA, HBsAg) được thực hiện trong khoảng thời gian từ 1 đến 3 tháng khi điều trị và lên đến 12 tháng sau ngừng ức chế miễn dịch bằng liệu pháp kháng vi rút theo yêu cầu nếu cần. Do sự đảo ngược huyết thanh HBsAg có thể dẫn đến viêm gan cấp tính gây tử vong, nên bắt đầu điều trị kháng virus ngay lập tức, không phụ thuộc vào mức ALT. Lưu ý, cả EASL và APASL đều khuyến cáo điều trị bệnh nhân HBV đã được hồi phục tương tự như bệnh nhân HBsAg dương tính nếu HBV-DNA huyết thanh ban đầu là dương tính.AGA phân loại bệnh nhân HBV đã hồi phục được điều trị bằng các thuốc ức chế miễn dịch truyền thống (ví dụ: thiopurines, methotrexate), CS liều thấp ≥ 4 tuần, CS nội khớp hoặc bất kỳ liều CS uống nào cho ≤ 1 tuần, là nguy cơ thấp (< 1%) đối với sự tái hoạt của virus viêm gan B và không khuyến cáo điều trị dự phòng, tương tự như các hướng dẫn khác của xã hội.
5. Nguy cơ nhiễm tái hoạt của virus viêm gan B ở bệnh nhân điều trị sinh học không nhắm mục tiêu TNF
Do ít dữ liệu về nguy cơ sự tái hoạt của virus viêm gan B ở những bệnh nhân điều trị sinh học không nhắm mục tiêu TNF, các tác giả đã xem xét tài liệu hiện có về nguy cơ sự tái hoạt của virus viêm gan B ở những bệnh nhân mắc bệnh tự miễn đã được sử dụng sinh học không nhắm mục tiêu TNF. Phần lớn các bài báo tập trung vào bệnh nhân HBV mãn tính hoặc nhiễm trùng đã giải quyết. Theo hướng dẫn của AGA, bệnh nhân HBV mãn tính và HBV đã hồi phục được điều trị bằng các liệu pháp nhắm mục tiêu không phải TNF được phân loại vào nhóm sự tái hoạt của virus nguy cơ trung bình và nên điều trị dự phòng.
Tuy nhiên, AASLD, EASL và APASL khuyến nghị theo dõi nối tiếp giữa các HBV đã hồi phục (nếu HBV DNA âm tính) với điều trị dự phòng trước nếu quan sát thấy sự tái hoạt của virus viêm gan B. Do đó, điều quan trọng là phải xác định chính xác sự tái hoạt của virus viêm gan B bằng các sinh phẩm không nhắm mục tiêu TNF.
Thông tin cần tư vấn liên hệ 0978342324 hoặc truy cập thuockedon24h.com để được hỗ trợ.


