Vai trò, ảnh hưởng thụ thể kết hợp với protein G trong các bệnh gan
Bài viết sau đây chúng ta cùng tìm hiểu về vai trò, ảnh hưởng của thụ thể kết hợp với protein G trong các bệnh gan thường gặp. Thụ thể kết hợp protein G được liên kết với các họ protein G riêng biệt, bao gồm Gs, Gi và Gq. Các protein Heterotrimeric G có liên quan đến tín hiệu của khoảng 800 thành viên trong thụ thể kết hợp với protein G. Một số con đường tín hiệu này đóng một vai trò quan trọng trong quá trình chuyển hóa của gan.
1. Vai trò của một số thụ thể kết hợp protein G trong các bệnh gan
Cho đến nay, một số thụ thể kết hợp protein G đã được chứng minh là có vai trò quan trọng trong các bệnh gan thường gặp. Một số thụ thể kết hợp với protein G quan trọng có giá trị lâm sàng tiềm năng ở các giai đoạn khác nhau của bệnh gan, từ NAFLD đến HCC. Ví dụ, GPR120 là một thụ thể chức năng cho các axit béo ω-3 có tác dụng chống viêm và kháng insulin mạnh.Vai trò của các thụ thể kết hợp với protein G trong các bệnh gan thường gặp như sau:
Bệnh gan
Thụ thể protein G
Biểu hiện
NAFLD / Steatosis
GPR120
Điều trị cpdA chủ vận GPR120 làm tăng độ nhạy insulin và dung nạp glucose và giảm nhiễm mỡ gan ở chuột béo phì do HFD
HCC
GPR49
GPR49 được thể hiện nhiều trong các dòng tế bào HCC của con người PLC / PRF / 5 và HepG2; sự biểu hiện quá mức của GPR49 trong mô HCC với sự đột biến của beta-catenin exon 3 cũng được hiển thị
Tổn thương gan / xơ hóa
GPBAR1
GPBAR1 là một bộ điều chỉnh ngược dòng biểu hiện trục của chemokine CCL2 và thụ thể CCR2 của nó trong giao diện của các tế bào hình sin gan
NASH / xơ hóa
GPR91
Succinate trong gan nhiễm mỡ có thể kích hoạt HSC thông qua thụ thể GPR91, dẫn đến tiến triển NASH
Chữ viết tắt: HCC: Ung thư biểu mô tế bào gan; HFD: Chế độ ăn nhiều chất béo; HSC: Tế bào hình sao gan; NAFLD: Bệnh gan nhiễm mỡ không do rượu.
Thụ thể kết hợp với protein G GPR49
GPR49, một thụ thể kết hợp với protein G với các phối tử không xác định, được biểu hiện nhiều trong các dòng tế bào ung thư biểu mô tế bào gan (HCC) của người PLC / PRF / 5 và HepG2. Ngoài ra, sự biểu hiện quá mức của GPR49 đã được hiển thị trong mô HCC với sự đột biến của beta-catenin exon ba. Một thụ thể thụ thể kết hợp với protein G đơn khác, GPR137, cũng được biểu hiện rộng rãi trong các dòng tế bào ung thư gan ở người, chẳng hạn như HepG2 và Bel7404. Sự suy giảm GPR137 do can thiệp RNA qua trung gian lentivirus trong hai dòng tế bào này đã ức chế đáng kể khả năng tăng sinh và hình thành khuẩn lạc. Việc hạ gục GPR137 trong tế bào HepG2 dẫn đến bắt giữ chu kỳ tế bào và quá trình chết rụng tế bào, cho thấy rằng việc nhắm mục tiêu GPR137 có thể ức chế sự phát triển của ung thư. Hơn nữa, sự biểu hiện thấp của GPR137 cho thấy sự tiến triển của HCC ở người và tỷ lệ sống sót thấp.
Thụ thể GPR132 hoặc G2A
Thụ thể GPR132 hoặc G2A là một thụ thể kết hợp với protein G cảm nhận proton và đóng một vai trò quan trọng trong chu kỳ tế bào và tăng sinh, sinh ung thư và đáp ứng miễn dịch. GPR132 cũng tham gia vào quá trình chuyển hóa lipid ở gan và hình thành sỏi mật ở chuột, vì những con chuột thiếu GPR132 được cho ăn chế độ ăn giàu chất xơ nhanh chóng phát triển sỏi mật và có chỉ số bão hòa cholesterol cao.
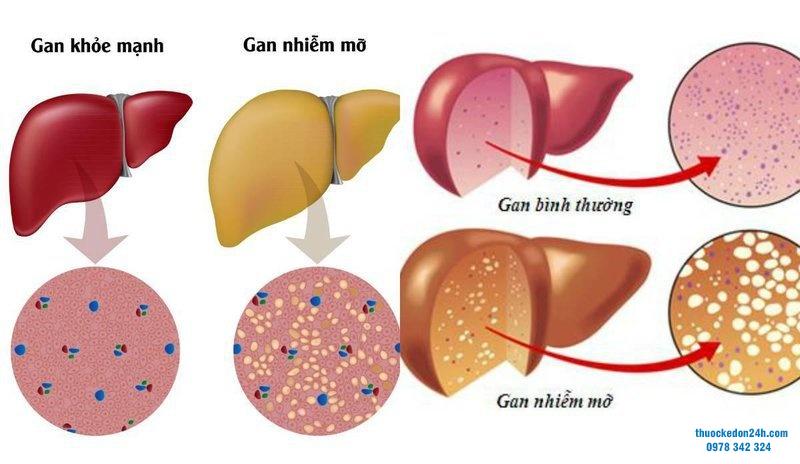
Succinate tăng lên ở các tế bào gan nhiễm mỡ
2. Không phải tất cả các thụ thể kết hợp protein G đều chống lại bệnh gan
Succinate tăng lên ở các tế bào gan nhiễm mỡ của chế độ ăn nhiều chất béo/ calo cộng với fructose và glucose cao ở chuột uống nước. Việc tiếp xúc với succinate đã điều chỉnh sự biểu hiện của GPR91 trong HSC sơ cấp và bất tử, làm tăng sự biểu hiện của các protein ECM của những tế bào này. Việc ức chế sự biểu hiện GPR91 bằng cách cho vi-rút chứa shRNA làm giảm kích hoạt HSC qua trung gian succinate. Trong khi đó, biểu hiện của GPR91 có tương quan với mức độ nghiêm trọng của xơ hóa trong các mẫu sinh thiết NASH ở người. GPR55 và phối tử nội sinh của nó, l-α-lysophosphatidylinositol có tương quan thuận với bệnh béo phì và bệnh tiểu đường loại 2 (T2D). Hơn nữa, thiếu GPR55 (GPR55 – / -) chuột cho thấy tín hiệu insulin bị suy giảm bằng chứng là giảm quá trình phosphoryl hóa protein kinase B và các mục tiêu hạ nguồn của nó, đồng thời có sự gia tăng đáng kể tổng lượng mỡ cơ thể và tổng hợp axit béo gan, có thể dẫn đến sự phát triển của nhiễm mỡ gan.
Trong cùng một nghiên cứu, tác giả cũng phát hiện ra rằng lysophosphatidylinositol đã kích hoạt tế bào gan H4IIE của chuột và tế bào gan HepG2 của người thông qua GPR55 để tăng cường quá trình phosphoryl hóa protein kinase B phụ thuộc insulin. Việc loại bỏ GPBAR1, một thụ thể kết hợp với protein G đối với BA thứ phát, làm tăng mức độ nghiêm trọng của tổn thương gan do acetaminophen. Hơn nữa, chủ nghĩa GPBAR1 làm trung gian cho sự biểu hiện trục của chemokine CCL2 và thụ thể CCR2 của nó trong giao diện của các tế bào hình sin gan.
3. Các protein điều hòa và tín hiệu thụ thể kết hợp với protein G
Nói chung, thụ thể kết hợp protein G được liên kết với các họ protein G riêng biệt, bao gồm Gs, Gi và Gq. Ví dụ, thụ thể glucagon được biểu hiện nhiều nhất trong tế bào gan được liên kết với các protein G kích thích, Gs. Các protein Heterotrimeric G có liên quan đến tín hiệu của khoảng 800 thành viên gia đình thụ thể kết hợp với protein G. Một số con đường tín hiệu này đóng một vai trò quan trọng trong quá trình chuyển hóa của gan. Ví dụ, cắt bỏ protein Gα 12 (Gα 12 ) làm tăng đáng kể sự tích tụ chất béo do đói trong gan của chuột và biểu hiện Gα 12 cũng giảm trong sinh thiết gan của bệnh nhân NAFLD.
Một nghiên cứu cơ học cho thấy rằng, Gα 12 điều hòa hô hấp của ty thể thông qua điều chỉnh sirtuin 1 và biểu hiện alpha của thụ thể được kích hoạt bởi peroxisome. Hơn nữa, sự biểu hiện của Gα 12 có liên quan đến thời gian sống thêm tổng thể của bệnh nhân HCC. Hiểu được vai trò của protein G trong gan cũng giúp mở ra vai trò của thụ thể kết hợp với protein G trong chuyển hóa gan và sự tiến triển của bệnh.
Một số thụ thể kết hợp protein G đã được chứng minh là có vai trò quan trọng trong các bệnh gan thường gặp.
4. Các cơ quan điều hòa protein tín hiệu G protein (RGS) điều chỉnh tiêu cực tín hiệu thụ thể kết hợp với protein G
RGS5 có thể bảo vệ chống lại NAFLD và NASH. Trong gan, RGS5 là một phân tử thiết yếu bảo vệ chống lại sự tiến triển của NAFLD. RGS5 liên kết trực tiếp với yếu tố tăng trưởng kinase 1 được kích hoạt bằng beta (TAK1) và ức chế quá trình phosphoryl hóa của nó và các con đường tiếp theo là c-Jun N-terminal kinase/ p38. RGS5 là một phân tử mục tiêu đầy hứa hẹn để tinh chỉnh hoạt động của yếu tố tăng trưởng chuyển đổi kinase 1 kích hoạt beta và xử lý NAFLD.HSCs được hoạt hóa là một trong những nguồn chính của nguyên bào sợi trong nhiều loại tổn thương gan, chúng tạo ra các protein ECM. Tín hiệu qua trung gian thụ thể kết hợp với protein G đóng một vai trò quan trọng trong việc co lại, di chuyển và kích hoạt HSC.
Ngoài ra tín hiệu của hầu hết các thụ thể kết hợp với protein G thông qua protein G được điều chỉnh bởi thụ thể kết hợp với protein G kinase (GRKs) cũng hoạt động trong cơ chế bệnh sinh của tổn thương gan. Ví dụ, chuột dị hợp tử GRK2 (GRK2 +/- ) cho thấy mức độ chất béo trung tính giảm và tỷ lệ trọng lượng gan trên cơ thể giảm so với chuột hoang dã khi được cho ăn chế độ ăn thiếu methionine và choline. Nồng độ protein GRK2 và mRNA tăng cũng được phát hiện trong sinh thiết gan của người nhiễm mỡ và bệnh nhân NASH. Hơn nữa, biểu hiện GRK2 cao phóng đại sự tích tụ lipid kích hoạt axit palmitic trong tế bào gan của người.
Thông tin cần tư vấn liên hệ 0978342324 hoặc truy cập thuockedon24h.com để được hỗ trợ.


